トップページ > 大学の技術・ノウハウ > マルチフォームデザインで創薬や食品分野に新たな可能性を持たせる固体脂質ナノ粒子 (ナノ粒子ドラッグデリバリーシステム)
| 資料 | |
|---|---|
| 組織名 | 東洋大学 理工学部生体医工学科/バイオ・ナノエレクトロニクス研究センター 前川 透 教授 |
| 技術分野 | 医工連携/ライフサイエンス |
| 概要 |
現在の医薬品開発において、薬物を最も有効で、副作用が少なく、患者に優しい製剤が求められています。そのため、薬物投与の最適化=薬物・成分を「必要とする部位」へ、「必要な量」で、「必要な時間」で送達させるためのドラッグデリバリーシステム(薬物送達システム、DDS)が、現在の薬物治療のみならず、今後発展が期待される遺伝子治療や再生医療においても不可欠な技術となっています。 本研究では、多孔構造の薬物(Cursin)内包ハイブリッド固体脂質ナノ粒子【Hybrid solid-lipid nanoparticles (HSLNs)】を合成し、粒子表面に2 種類の分子で修飾する事に成功し、投薬治療が難しいとされている脳腫瘍の治療に有効に働くこと(脳関門の通過・脳腫瘍への特異的結合・薬の投与・脳腫瘍の縮小・延命)を実証しました。 |
| お問い合わせ |
この技術・ノウハウに関するお問い合わせ |
| 詳細 | |
簡略図
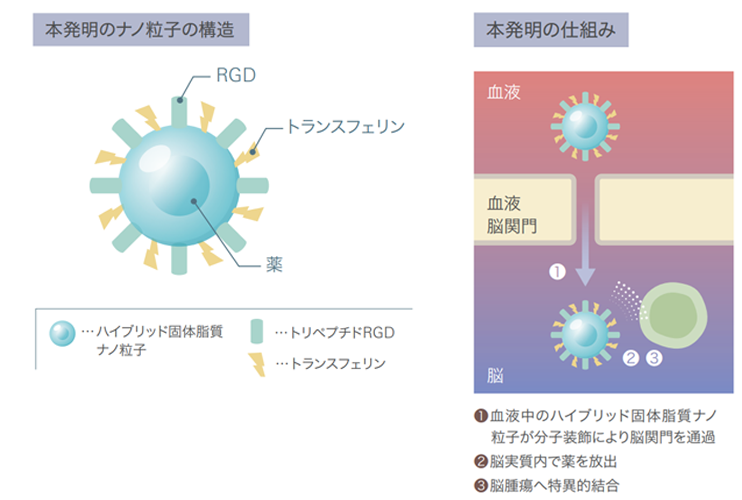
| 粒子表面修飾分子を適切に選択することにより、他の種類の腫瘍への特異的結合が実現できるという点がマルチフォームデザインなナノ粒子ドラッグデリバリーシステムです。 |
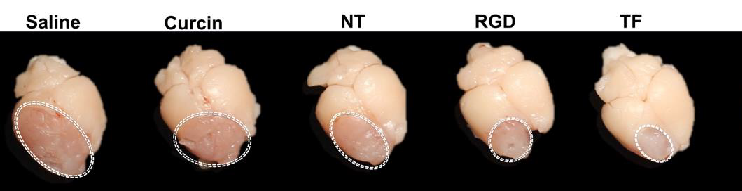
| クルシンのみを投与した群(Curcin)の脳試料では、ほぼ1つのローブ全体が腫瘍化していた。一方、本技術のナノ粒子を投与した群(DUAL)は最も治療が成功した群であり、肉眼で確認できる腫瘍は脳の表面には認められなかった。 |
背景
現在、薬物による治療は定期的な服用や筋肉および静脈への注射によって全身へ投与する方法がとられています。注射による投与は疼痛や組織傷害を引き起こすことがあり、経口投与は性別、年齢および病状など個体差に応じた投与が難しいとされています。また、投与された薬物は目標患部のみでなく正常細胞(組織)にも分布し、肝臓の代謝などにより減少するため、投与量のごく一部しか目標患部に達しない、また複数の血液関門が存在する患部おいては目標患部薬剤が達しないことにより作用しないため、正常細胞に分散した薬物は、副作用の原因となります。そのため、薬物の1回の服用や注射だけでは長時間有効な血中濃度を維持できず、必要量よりはるかに多くの量を繰り返し投与しなければならないという課題があります。
近年、薬物投与の最適化=薬物・成分を「必要とする部位」へ、「必要な量」で、「必要な時間」で送達させるため、ドラッグデリバリーシステム(薬物送達システム、DDS)が、現在の薬物治療のみならず、今後発展が期待される遺伝子治療や再生医療においても不可欠な技術となっています。
本研究では、多孔構造の薬物(Cursin)内包ハイブリッド固体脂質ナノ粒子【Hybrid solid-lipid nanoparticles (HSLNs)】を合成し、粒子表面に2 種類の分子で修飾する事に成功し、投薬治療が難しいとされるが脳腫瘍の治療に有効に働くこと(脳関門の通過・脳腫瘍への特異的結合・薬の投与・脳腫瘍の縮小・延命)を実証しました。
技術内容
◎新たなドラッグデリバリーシステム
ドラッグデリバリーシステムは、治療に必要な薬物・成分を「必要とする部位」へ、「必要な量」で、「必要な時間」で送達させるため技術の総称です。本研究では、人体に異物が侵入したときに、体内で生成される抗体に着目。抗体がもつ、患部に含まれる特定の抗原に特異的に反応するという性質を薬の運搬に応用することを考えました。ナノテクノロジーで私たちが開発した独自のナノ粒子に抗がん剤を内包し、その表面を二種類の抗体分子で修飾(コーティング)しています。またナノ粒子は多孔質であり、さらに二重膜構造となっているため、薬はゆっくりと血液中に浸透していきます。他の正常細胞への影響を最小限に抑え、安全に目標の患部まで薬を届けることができます。
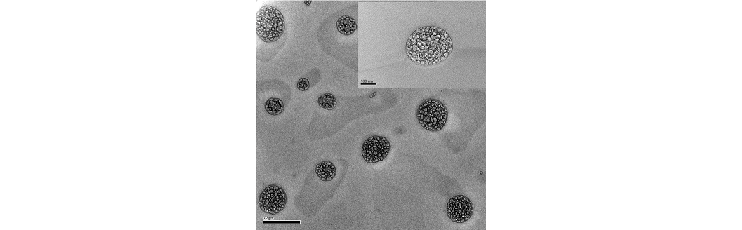
本ナノ粒子の細胞毒性については、本ナノ粒子をヒト臍帯静脈内皮細胞(HUVEC)、ヒト皮質神経細胞株(HCN-1A)及びグリオーマ細胞株(Gl-1)を使用し、各細胞の培地に、0(対照)、1、10及び100μg/mLのナノ粒子を添加し、72時間培養し、MTTアッセイにより各細胞の生存率を測定した結果、様々な細胞に対して細胞毒性が低く、細胞適合性があることが明らかとなっています。
◎脳の障壁を突破するドラッグデリバリーシステムの実現
脳には血液中からの異物の侵入を防ぐ「血液脳関門」という障壁があります。そのため、脳腫瘍まで抗がん剤が届くことは、これまでほとんどありませんでした。本技術により「トランスフェリン」と「RGD」という二種類の分子をある一定の割合でナノ粒子に装飾し、血液脳関門を突破して効率よく患部まで到達することに成功しました。さらに、抗がん剤を粒子に内包することで、薬剤の毒性が抑えられ、生体適合性も向上するという利点もあります。
このナノ粒子は、表面の分子を変えるだけで、安全性を保ったまま他の臓器の治療に応用することが可能です。現在は医学を専門とする先生方とも連携を図り、すい臓がん治療への展開を検討しています。
◎幅広い分野での応用が可能な内包ハイブリッド固体脂質ナノ粒子
このナノ粒子は、細胞毒性が低い事から、食品分野やサプリメント等のヘルスケア分野への応用も期待できる可能性があります。
◎粒子の動きを可視化する「生体イメージング」への可能性
このナノ粒子で特徴的なのが、抗がん剤以外の多様な物質を内包できるため、量子ドットと呼ばれる2-10ナノメートル程度の非常に小さな結晶を内包するナノ粒子を開発し、この量子ドットをナノ粒子内に取り入れることで、粒子の動きを可視化する「生体イメージング」が可能となります。
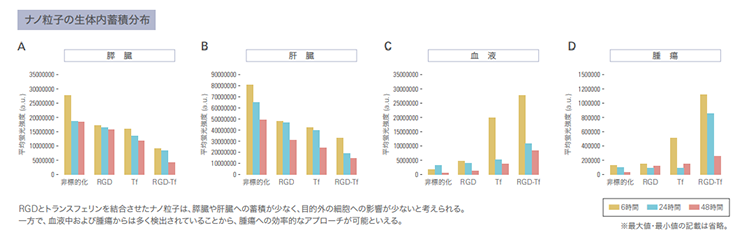
例えば、本量子ドットによる生体イメージングを活用し、トランスフェリンとRGDを修飾させたナノ粒子の蛍光強度を計測した結果、本ナノ粒子が膵臓や肝臓への蓄積が少なく、目的外の細胞への影響が少なく、さらに、血液中および腫瘍からは多く検出されていることから、腫瘍への効率的なアプローチが可能という事が明らかになりました。
※関連する発表論文・特許名称・出願番号等
・特許第 6321305 号 薬物送達用ナノ粒子組成物
・US10765637B2 RGD and transferrin nanoparticle composition
技術・ノウハウの強み(新規性、優位性、有用性)
連携企業のイメージ
技術・ノウハウの活用シーン(イメージ)
技術・ノウハウの活用の流れ
まずは、研究者とのご面談を調整させていただきます。 その上で、ナノ粒子化・修飾条件の検討を研究室で行う事が可能です。
専門用語の解説
ドラッグデリバリーシステム
体内での薬物分布を制御することで、薬物の効果を最大限に高め、副作用を最小限に抑えることを目的とした技術の総称。
正常細胞
体や周囲の状態に応じて、ふえたり、又はふえることをやめたりする、正常な働きをしている細胞。
トランスフェリン
血漿に含まれるタンパク質の一種。鉄イオンを結合し、その輸送を担っている。
RGD
Arg-Gly-Asp配列を有するタンパク質。
メールフォームのご利用は、以下の項目にご記入のうえ「送信する」ボタンを押してください。
担当者より折り返しご連絡いたします。
個人情報の取り扱いについては、こちらをご覧ください。
![]()